

课题组简介
干细胞毒理学课题组利用多能干细胞重点探索传统、新型环境污染物的健康效应问题,并构建胚胎毒性、发育毒性、生殖毒性和功能毒性的实验模型,致力于研究目前环境污染物的健康危害及致毒机制,提出有效的预防与防治措施。
干细胞毒理学课题组组长Francesco Faiola研究员在干细胞生物学、分子生物学和生物化学等领域具备深厚的研究背景。2014年入选中国科学院“百人计划”,是生态环境研究中心引进的第一位外籍研究员。目前主要从事污染物的干细胞毒理学研究,在中科院生态环境研究中心建立国际上率先使用干细胞进行环境毒理学研究的课题组。
课题组承担了包括“中科院战略性先导科技专项B类”、国家自然科学基金面上项目等多项科研项目,并且密切围绕上述项目展开了多项科研工作。
(一)建立了一系列干细胞毒理学研究模型。
1) 成功建立了小鼠多能干细胞胚胎毒性、发育毒性和细胞功能毒性检测相关实验模型。
2) 成功构建了人源胚胎干细胞拟胚体分化模型,优化了拟胚体形成过程,建立了较为完整的胚胎干细胞三胚层多向分化毒性评估体系。
3) 使用人源胚胎干细胞,构建了包括心脏细胞、肝脏细胞、神经/胶质前体细胞、胰腺前体细胞、肺泡细胞和皮肤细胞在内的多种人源脏器细胞分化模型,并根据环境毒理学研究的需要优化了实验条件,确定了发育毒性和功能毒性评价指标,最终建立了一系列基于人源胚胎干细胞定向诱导分化过程的毒理学研究体系(图1)。
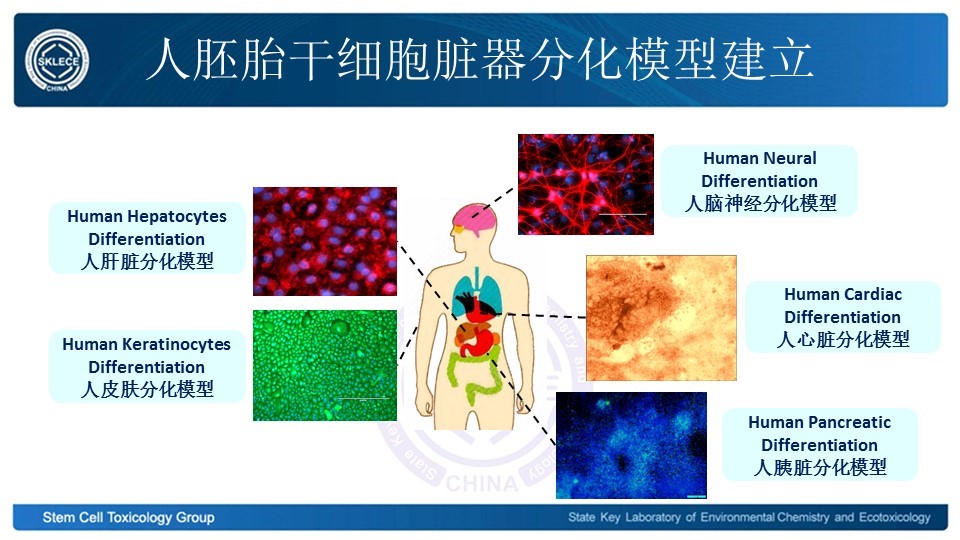
图1 人胚胎干细胞脏器分化模型建立
课题组建立的多种适用于环境毒理学的实验模型,已得广泛应用。特别是人源胚胎干细胞分化模型,可极大程度上贴合真实人体脏器发育过程,解决了传统动物实验结果外推至人类健康风险存在偏差的问题,并且大大降低了动物实验量,避免动物伦理问题。同时,体外细胞实验相对简便、快速和经济,降低了评估化合物毒性的成本,缩短了实验周期。课题组建立的各种干细胞毒理学评价模型,推进了干细胞在毒理学研究领域的应用,为评估药物或环境污染物对人体各个阶段不同器官的发育和功能毒性奠定基础,同时也为将来实现化合物毒性评估的高通量化提供技术支持。
(二)应用干细胞毒理学研究模型,评估了多种典型环境污染物的发育毒性。
1) 基于小鼠胚胎干细胞模型的双酚类化合物神经发育毒性研究
基于小鼠胚胎干细胞拟胚体分化,通过撤除干细胞培养基中LIF,诱导胚胎干细胞分化为三维聚合体状的拟胚体(Embryonic Body,EB),进一步模拟体内发育过程向三胚层(内胚层、中胚层、外胚层)进行分化。课题组研究结果显示,在胚胎干细胞自发分化过程中,10 μM的BPA对中胚层影响微乎其微,相关标志基因T、Hand1无明显变化。在连续20天自发分化的过程中,10 μM的BPA对内胚层及外胚层的发育均有影响,特别是对神经外胚层的影响格外显著,相关标志基因Sox1、Pax6、Sox3、Nestin均受到显著抑制。该项研究证实,BPA可通过抑制小鼠神经外胚层相关基因的表达,从而造成神经系统发育障碍,BPA神经发育毒性作用不容忽视。由于结构类似,BPF和BPS在相同实验条件下,表现出与BPA相似的毒性效应。实验结果已初步证实三种化合物对神经发育过程中的轴突导向产生明显干扰,进一步造成神经发育毒性的发生。
2) 基于小鼠胚胎干细胞模型的DEP/DBP神经发育毒性研究
邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二丁酯(DBP)广泛应用于塑料制品及个人护理用品和化妆品中,可通过呼吸、饮食和皮肤接触等途径进入人体内,产生毒性效应。课题组研究表明,高浓度的DEP/DBP可降低小鼠胚胎干细胞(mESC)细胞活力,并引起mESC胞内ROS累积;DBP还可损伤mESC膜完整性(胞外LDH累积)并激活Caspase-3/7。低浓度DEP/DBP(非细胞毒性剂量)可干扰mESC自发分化,外、中、内三个胚层的标记基因表达水平均受到了影响,且DEP和DBP对神经外胚层基因的表达水平影响最为普遍,具体表现为Fgf5、Otx2、Pax6、Nestin、Sox1、Sox3等神经发育相关的基因均显著上调。
3) TBBPA及类似物对胚胎神经发育影响的研究
TBBPA是广泛使用的溴代阻燃剂,多添加在建筑材料,纺织品类以及塑料制品等中。TBBPS和TCBPA与TBBPA具有相似的结构,作为其替代物使用。目前TBBPS和TCBPA胚胎发育毒性的评估数据有限,其对发育的影响未知。课题组使用小鼠胚胎干细胞神经分化模型研究了TBBPA及其类似物的发育神经毒性,结果发现,TBBPA和TBBPS上调神经前体细胞标志基因(Sox1、Sox3和Pax6)以及神经元基因(Map2和NeuroD)的表达,但TCBPA 显著地抑制这些基因的表达。对神经前体细胞标志蛋白MAP2的免疫染色结果显示,TBBPA 和TBBPS处理组神经前体细胞数增多,TCBPA处理组神经前体细胞显著减少,此结果再次证实三种污染物对神经分化的影响。进一步分子水平研究发现,TBBPA类化合物对Notch和Wnt信号通路的影响存在差异。TBBPA处理促进Notch通路效应因子的表达,但不显著影响Wnt通路靶基因Axin2和Lef1的表达,暗示TBBPA可能通过上调Notch信号通路促进神经分化。与上述结果相反的是TBBPS显著下调Axin2和Lef1的表达,但是对Notch通路效应因子的影响不显著,因此TBBPS可能通过抑制WNT通路从而促进神经异常分化。TCBPA促进Hes1和Hes5的表达并且同时抑制Axin2和Lef1的表达,最终抑制了神经分化。
4)全氟化合物对人胚胎干细胞胰腺分化影响的研究
目前的一些流行病学研究显示,PFOA和PFOS暴露与糖代谢紊乱和糖尿病发生之间具有相关性,并且一些动物实验的结果显示PFOS暴露会影响胰腺器官的形成,可能导致I型糖尿病的发生。然而,由于在哺乳动物中很难追踪研究环境污染物对胰腺发育的影响,因此目前已有研究能够证明PFOA和PFOS暴露可以干扰胰腺发育的证据并不充足。课题组建立了人胚胎干细胞胰腺分化模型,通过检测胰腺分化过程中不同阶段标志基因的表达水平来判断胰腺分化是否受到影响。实验结果显示,经过13天诱导和污染物暴露后,PFOA和PFOS显著抑制胰腺发育相关基因表达,表现为:限定性内胚层标志基因FOXA1、FOXA2、SOX7和SOX17,原肠期共同介导胰腺前体形成的转录因子HNF1b、HNF4a和HNF6,胰腺前体细胞的转录因子PDX1和SOX9各标志性基因水平降低。这一部分实验结果表明,与人体暴露剂量相接近的5 nM PFOA或PFOS即对胰腺发育具有显著的抑制作用(图3)。该项研究成果与已有动物实验数据相吻合,暗示PFOA和PFOS可能在胚胎发育早期阶段干扰胰腺的正常发育。
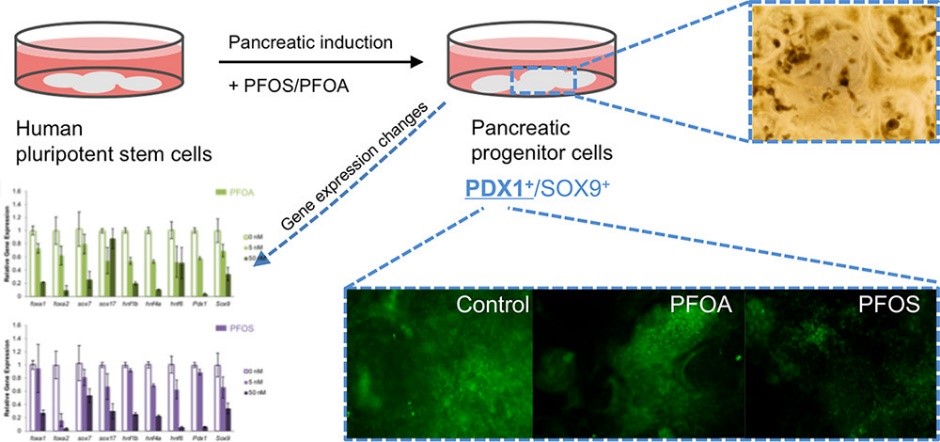
图 3 PFOA和PFOS抑制早期胰腺发育
截至目前,课题组研究发现了大量环境污染物如双酚类化合物、卤代双酚类化合物、多溴联苯醚、全氟化合物、纳米银和纳米碳等的健康风险效应,为阐明化合物结构与毒性效应之间的关系提供有力证据。此外,结合传统的毒理学研究手段与高通量测序技术,初步揭示了上述化合物的致毒机理,例如多溴联苯醚可能通过影响甲状腺素受体相关信号通路从而引起发育肝脏毒性,全氟化合物可能通过激活WNT信号通路从而干扰心脏分化。上述化合物致毒机理的揭示,为制定相应的解毒策略提供了科学依据。
(三)研究了Nac1 对体细胞重编程的影响
在基础生物学方面,课题组与美国西奈山伊坎医学院Jianlong Wang课题组开展合作研究,发现转录因子Nac1参与调控体细胞重编程,该项研究是体细胞重编程分子机制研究的突破性成果。多能性干细胞能够转化为体内的任何一种类型的细胞,典型的多能性干细胞包括胚胎干细胞(ESCs)和诱导多能干细胞(iPSCs)。胚胎干细胞分离自哺乳动物胚胎早期的内细胞团,诱导多能干细胞是通过细胞核重编程,将已终末分化的、仅具有单一潜能的体细胞转变为可多向分化的、具有多能分化特性的细胞。诱导多能干细胞与胚胎干细胞具有类似的特性,可分化为三胚层,亦可产生原始生殖细胞(PGCs)。因此,诱导多能干细胞具有替代胚胎干细胞的能力,不仅可避免医学上使用胚胎干细胞存在的伦理问题,还可为细胞治疗、自体医疗、药物筛选以及毒理学研究提供有利帮助。Nac1表达的蛋白最初发现于大鼠脑的伏核中,多种癌症细胞中也存在高表达。在胚胎干细胞中,Nac1与多种干细胞因子具有相互作用,特别是和多能性相关的Nanog,以及重编程因子Oct4、Sox2均具有相互作用,但这些因子间的相互作用过程及机制尚未阐明。Faiola课题组研究证实转录因子Nac1通过调节粘附因子E-cadherin的表达,进而影响体细胞重编程过程。Nac1下调E-cadherin的阻抑基因Zeb1,直接作用于基因位点抑制转录,并间接通过影响miR200家族从而调控Zeb1的mRNA水平(图5)。该项研究在体细胞重编程的分子机制研究方面取得长足进展,是中国和美国科研团队通过国际合作在干细胞生物学基础研究方面取得的突破性成果。
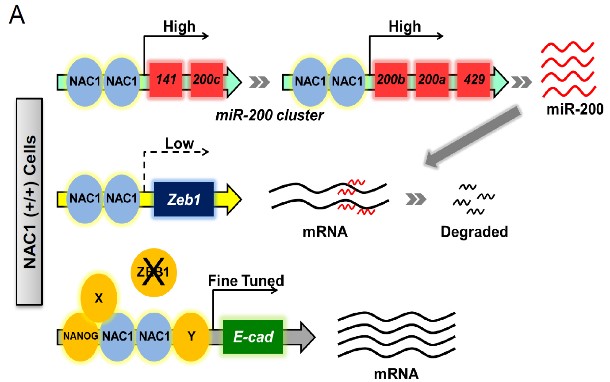
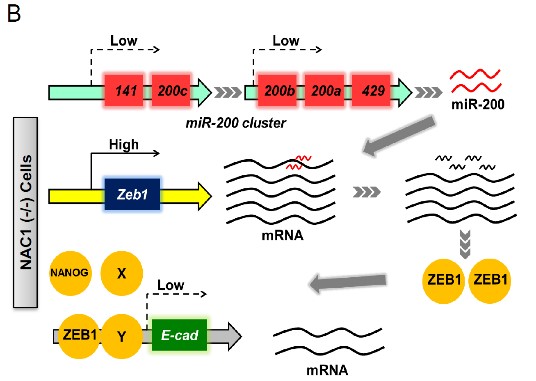
图5:Nac1调节Zeb1和E-cadherin介导的重编程
(A):Nac1表达情况下体细胞重编程示意图
(B):Nac1缺失情况下体细胞重编程示意图
干细胞毒理学组成员风貌:
