

曲广波等揭示PFAS直接作用靶点及毒性早期分子事件
中国科学院生态环境研究中心环境化学与环境毒理全国重点实验室曲广波研究员、刘娴副研究员与中国科学院大连化学物理研究所叶明亮研究员团队合作,在全氟和多氟烷基物质(PFAS)毒性机制研究方面取得新进展。相关成果以“Applying Thermal Proteome Profiling to Per- and Polyfluoroalkyl Substances (PFAS): Proteome-Wide Identification of Molecular Targets and Early Events”为题,发表于Environmental Science & Technology期刊。
全氟和多氟烷基物质(PFAS)是一类广泛应用于工业和消费品中的持久性有机污染物,具有高度稳定性和生物蓄积性。流行病学和实验研究表明,PFAS暴露与肝脏损伤、代谢紊乱、免疫抑制及肿瘤等健康风险密切相关。但目前对PFAS作用的直接蛋白靶点认知仍极度缺乏。
研究团队基于热蛋白质组学(TPP)技术,对五种代表性PFAS,包括PFOA、PFOS、PFNA、PFDA以及替代物GenX,开展了蛋白质组水平的直接作用靶点解析。结果显示,PFAS可在全蛋白质组范围内诱导蛋白热稳定性变化,共鉴定出173个潜在直接作用靶点,显著拓展了传统以核受体为核心的毒性研究框架,为识别PFAS的分子起始事件提供了全新的研究路径。
研究发现,传统长链PFAS在靶点上呈现一定共性,均可作用于小GTP酶SAR1A和SAR1B,提示其可能通过调控mTORC1信号通路影响细胞代谢与增殖。相比之下,替代型PFAS GenX表现出明显不同的靶点特征,其特异性作用于WDR89等蛋白,提示其可能通过染色质调控和蛋白复合体组装等非核受体途径发挥毒性效应。
进一步结合细胞热迁移实验(CETSA)和分子对接分析,研究验证了关键蛋白与PFAS之间的直接结合关系,并从结构层面解释了不同PFAS的靶点选择性差异。基于Comparative Toxicogenomics Database(CTD)数据库的整合分析,研究还将PFAS相关直接作用靶点与279种疾病建立关联,发现其潜在健康影响主要涉及消化系统疾病和心血管疾病等领域。该研究从蛋白质组尺度系统揭示了PFAS的直接作用靶点及毒性早期分子事件,为深入理解PFAS健康风险提供了关键证据,也为新型污染物的机制导向风险评估与优先管控提供了重要科学依据。
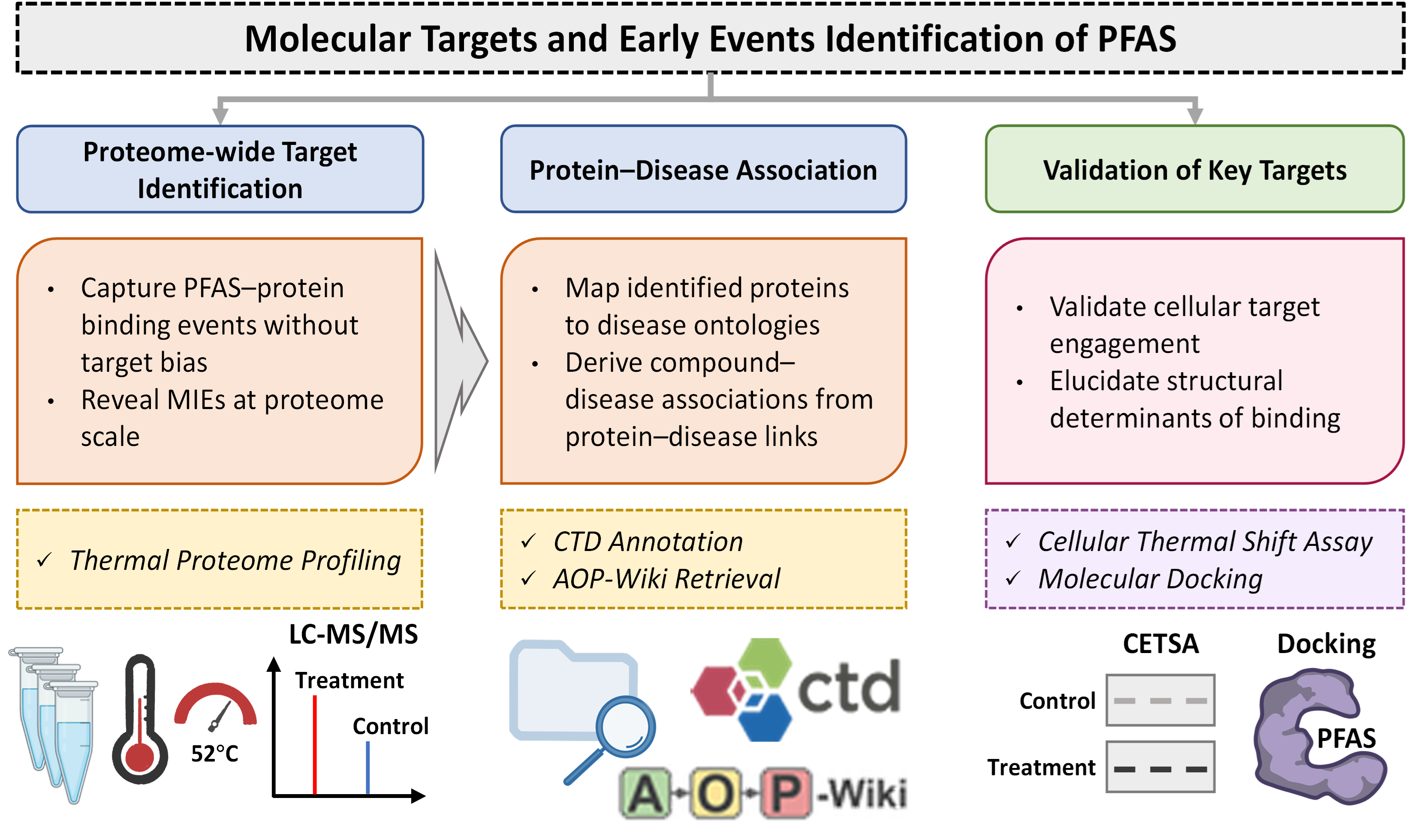
图1 PFAS直接作用靶点识别与验证整体研究框架
浙江大学联合培养博士生郑雪寒与中国科学院大连化学物理研究所李亚楠博士为论文共同第一作者,中国科学院生态环境研究中心刘娴副研究员与中国科学院大连化学物理研究所叶明亮研究员为论文共同通讯作者。该研究得到了国家重点研发计划、国家杰出青年基金、中国科学院战略性先导科技专项等项目的支持。
论文链接:https://doi.org/10.1021/acs.est.5c15707