

王亚韡组在PFAS的人体赋存、传输和消除领域取得新进展
2023年6月19 日,王亚韡组在PFAS人体赋存、传输和消除领域取得新进展,相关结果以“A critical review on the bioaccumulation, transportation, and elimination of per- and polyfluoroalkyl substances in human beings”为题(DOI: 10.1080/10643389.2023.2223118)在线发表于环境科学领域权威期刊Critical Reviews in Environmental Science and Technology上。
全氟及多氟烷基类化合物(Per-and polyfluoroalkyl substances, PFAS)是目前受到国际社会广泛关注的一类人为生产的化合物。由于其具有持久性、生物富集性、长距离迁移性、毒性等特性,PFAS的典型单体及其相关化合物已经被列入各环境国际公约进行全球管控。PFAS无处不在,流行病学和生物组学的结果显示,PFAS暴露与人体健康密切相关。了解PFAS在人体中的赋存、传输及消除的行为和生物学机制有助于明晰PFAS的人体健康风险,并为PFAS的国际管控提供数据支持。
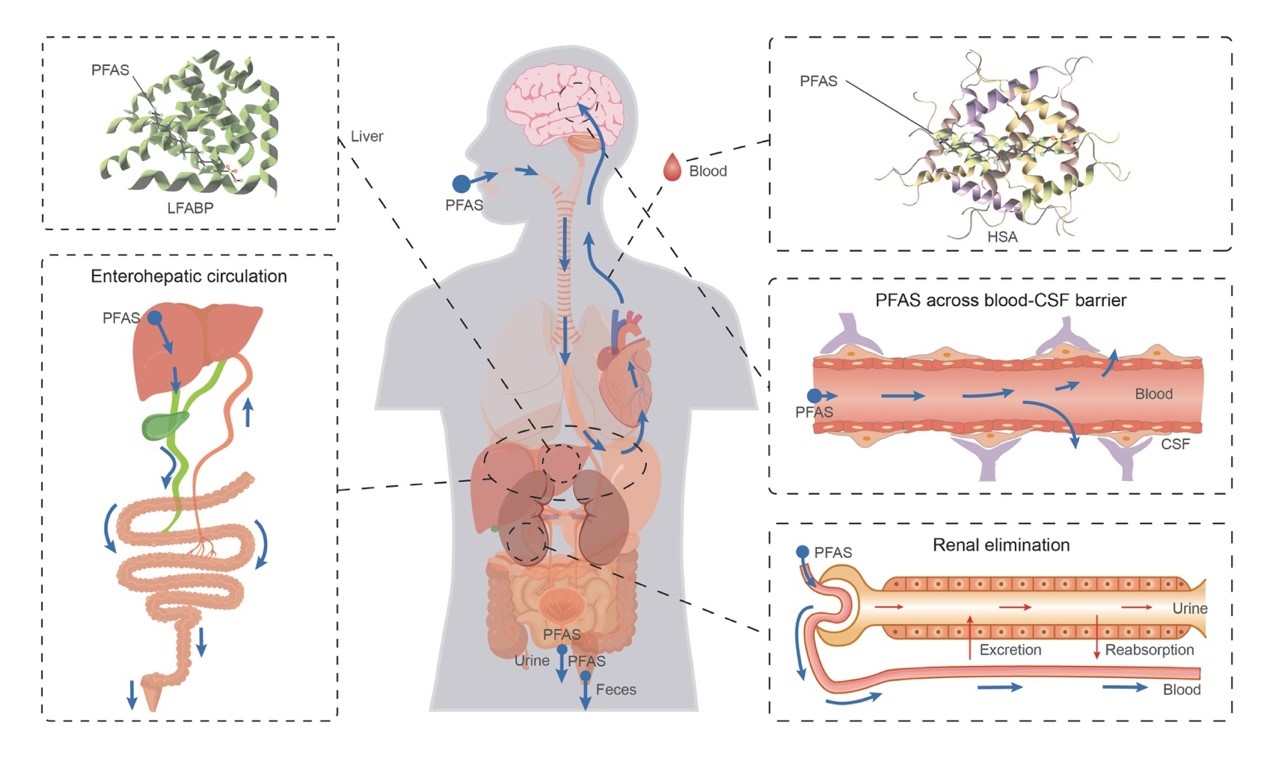
图1 论文TOC
本文系统总结了PFAS在人体内的赋存、传输及消除行为和机制(图1),并使用分子对接的计算手段,计算了56种典型PFAS单体和4种肾脏传输蛋白的结合能力,进一步探索了PFAS肾脏消除的规律。
血液和尿液是研究PFAS人体内赋存水平的重要基质,由于伦理学的限制,目前关于PFAS在人体器官内的报道非常匮乏,仅有的少量研究显示,肝脏、肾脏和肺是PFAS主要的人体赋存器官;PFAS倾向于与蛋白结合,作为人体血液和肝脏中的主要蛋白,现有的研究主要关注PFAS与血液和肝脏中主要蛋白——人体血清白蛋白(HSA)和肝脏脂肪酸结合蛋白(LFABP)的分子结合机制,相关研究表明PFAS与两种蛋白的结合能力与PFAS的链长密切相关(图2);母婴传输是PFAS在人体内传输的重要过程,PFAS的母婴传输效率与PFAS的链长密切相关。少量研究报道了PFAS跨越血脑屏障的行为,但人体内PFAS传输过程和机制的研究十分匮乏(图2);关于PFAS的人体消除行为的研究主要集中在PFAS人体半衰期的估算与代谢,但PFAS的人体肾脏传输机制的研究目前十分匮乏;有少量研究建立了PFAS典型单体在人体内的生理药代动力学( physiologically based pharmacokinetic, PBPK)模型,但关于新型PFAS在人体内的PBPK模型还尚未被报道。
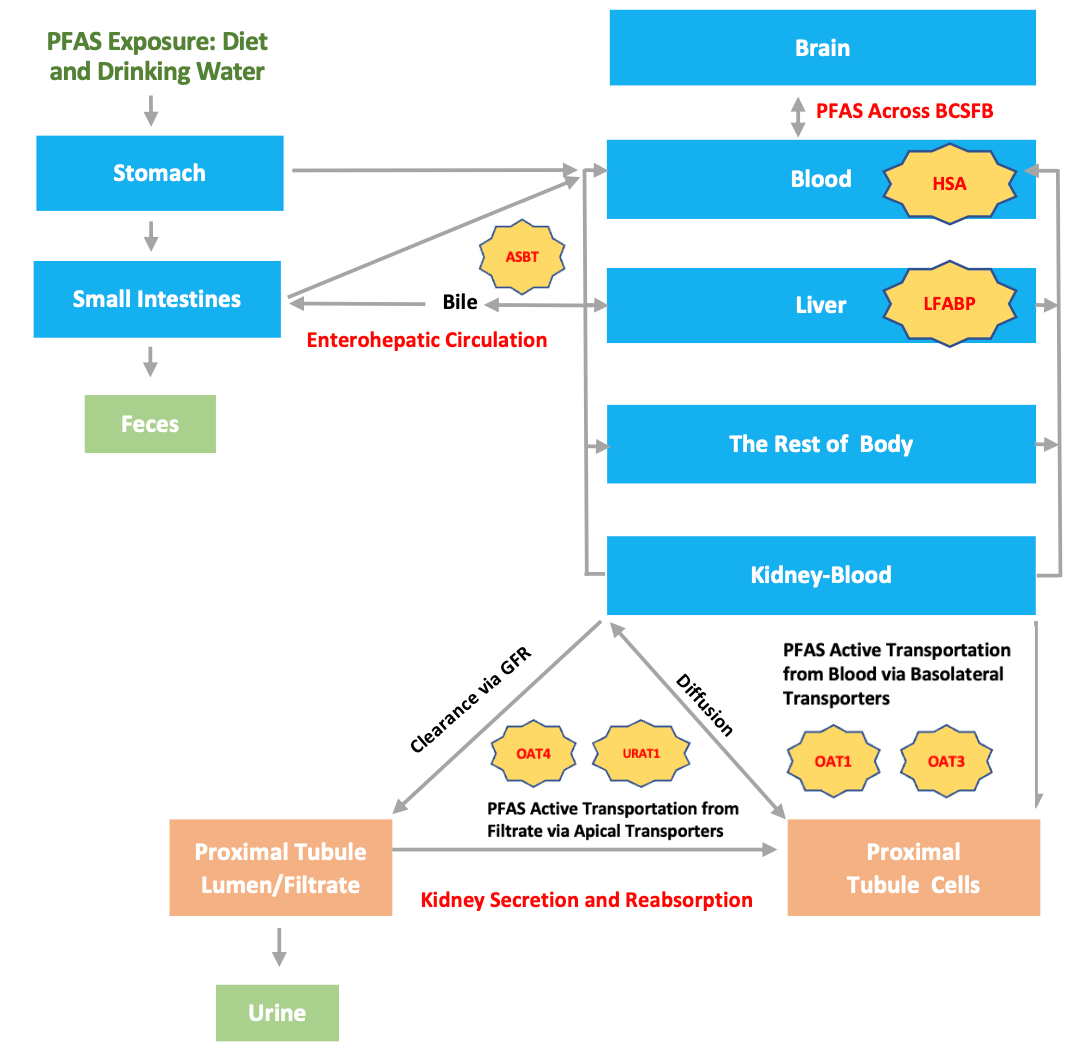
图2 PFAS在人体内的赋存、传输及消除机制简图
为了探索PFAS的人体肾脏传输的规律,作者使用分子对接的手段计算了56种PFAS典型单体与4种肾脏传输蛋白(OAT1,OAT3,OAT4和URAT1)的结合能力。研究结果显示大多数的PFAS单体与4种蛋白存在结合,这说明PFAS与四种蛋白的结合会影响PFAS的肾脏传输行为(图3)。
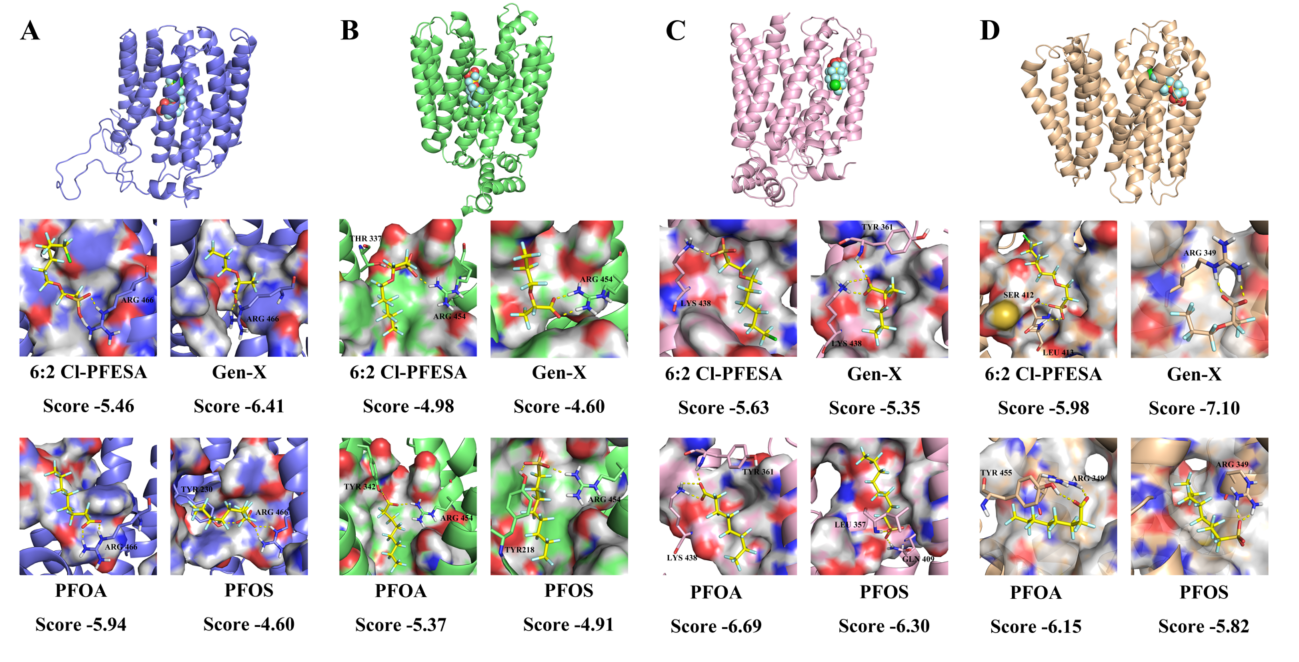
图3 四种典型PFAS单体(PFOS, PFOA, Gen-X和6:2 Cl-PFESA)与四种肾脏传输蛋白(OAT1,OAT3,OAT4和URAT1)的分子对接结果示意图
文章结尾为未来相关研究进行了展望,包括使用非靶向检测技术揭示更多PFAS单体在人体内的赋存情况,探索PFAS与人体内其它重要蛋白的结合能力,关注PFAS的肝肠循环过程、跨越胎盘屏障的过程,使用实验结合计算机模拟的新型研究手段,建立新型PFAS在人体内的PBPK模型,开展大范围大尺度的合作研究等。
该论文的第一作者为卢瑶,通讯作者为赵春燕教授、王亚韡研究员。该研究得到了国家自然科学基金项目、 卢嘉锡教育科学基金、中国博士后科学基金等项目的支持。
原文链接:
http://dx.doi.org/10.1080/10643389.2023.2223118